
VANTAGENS E LIMITAÇÕES DAS BATERIAS DE LÍTIO-ÍON
É a tecnologia mais recente. Está tendo um rápido crescimento. A bateria de lítio-íon é conhecida como Li-Ion (do Inglês “lithium-ion”). É usada quando se deseja alta densidade de energia e peso leve. Uma célula de Li-Ion é composta de quatro partes principais:

- Catodo (ou terminal positivo)
- Anodo (ou terminal negativo)
- Eletrólito
- Separador poroso
O catodo varia entre diferentes tipos de células, mas é sempre um composto de lítio misturado com outros materiais. O anodo é quase sempre grafite e às vezes inclui vestígios de outros elementos. O eletrólito é geralmente um composto orgânico contendo sais de lítio para transferir íons de lítio. O separador poroso permite que íons de lítio passem através dele enquanto separa o anodo e catodo dentro da célula.
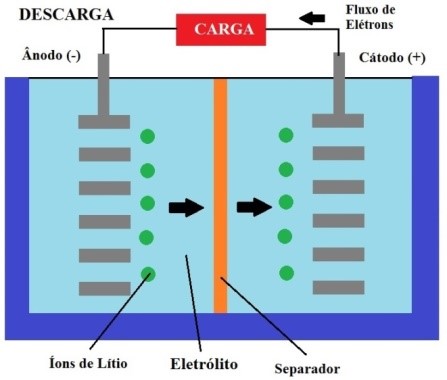
Figura 2 - Baterias de Li-Ion – descarga
Quando a célula é descarregada, íons de lítio se movem do anodo para o catodo passando pelo eletrólito. Isso descarrega elétrons no lado do anodo, alimentando a carga, conforme ilustrado na figura 2.
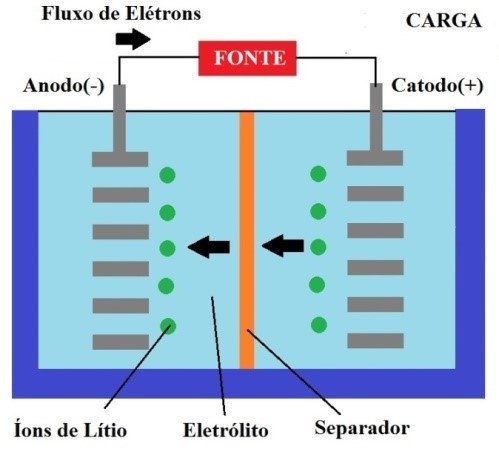
Figura 3 - Baterias de Li-Ion – carga
Quando a célula é recarregada, este processo é invertido e os íons de lítio passam de volta do catodo para o anodo, conforme figura 3.
Essas baterias são mais caras que as outras e precisam ser utilizadas dentro de padrões rígidos de segurança. Aplicações incluem notebooks e telefones celulares.
O lítio é o mais leve de todos os metais usados em baterias, tem o maior potencial eletroquímico e fornece a maior densidade de energia por peso.
Baterias recarregáveis que usam anodos de metal de lítio (eletrodos negativos) são capazes de fornecer tanto alta tensão quanto excelente capacidade, resultando em uma grande densidade de energia.
Depois de muita pesquisa com baterias recarregáveis de lítio durante os anos 80, foi descoberto que o ciclo de carga e descarga causava mudanças no eletrodo de lítio. Essas transformações reduzem a estabilidade térmica, causando potenciais condições de fuga térmica.
Quando isso ocorria, a temperatura da célula rapidamente se aproximava do ponto de derretimento do lítio, resultando em uma violenta reação chamada “abertura com chama”. Uma grande quantidade de baterias de lítio recarregáveis enviadas ao Japão teve que regressar em 1991 depois de uma bateria em um telefone celular liberar gases inflamáveis e causar danos no rosto da pessoa.
Por causa da instabilidade inerente do metal de lítio, especialmente durante o carregamento, pesquisas conduziram para uma bateria de lítio não metálica que usa íons de lítio.
Embora pouco menor em densidade de energia do que a bateria de metal de lítio, a bateria de Li-Ion é segura, tomadas certas precauções quando carregando e descarregando.
Em 1991 a SONY comercializou a primeira bateria de Li-Ion. Outros fabricantes também se adaptaram à tecnologia. Hoje, a Li-Ion é a bateria que mais está crescendo e é a química de bateria mais promissora.
A densidade de energia da bateria de Li-Ion é tipicamente o dobro das de NiCd padrão. Melhorias nos materiais de eletrodo ativo têm o potencial de aumentar a densidade de energia perto de três vezes em relação às de NiCd.
Além da alta capacidade, as características de carga são razoavelmente boas e se comportam como as de NiCd em termos de características de descarga, com forma similar do perfil de descarga, mas com tensão diferente. A curva de descarga plana oferece utilização eficiente da energia armazenada em um espectro de tensão desejável.
A bateria de Li-Ion é de baixa manutenção, uma vantagem que a maioria das outras químicas não tem. Não existe memória e nenhum ciclo programado é exigido para prolongar a vida da bateria. Além disso, a autodescarga é menor que a metade se comparada com as baterias de NiCd e NiMh.
A alta tensão da célula de Li-Ion, acima de 3V, permite a fabricação de conjuntos de baterias que consistem em apenas uma célula. Muitos dos telefones móveis de hoje funcionam com uma célula simples, uma vantagem que simplifica o projeto dos equipamentos. As tensões de alimentação de aplicações eletrônicas têm caído, o que requer poucas células por conjunto de baterias. Para manter a mesma energia, contudo, são necessárias maiores correntes. Isto enfatiza a importância de uma resistência muito baixa da célula para permitir fluxo de corrente elevado.
Apesar de suas vantagens, as baterias de Li-Ion também têm as suas inconveniências. Ela é frágil e requer um circuito de proteção para manter uma operação segura. Embutido dentro de cada conjunto, o circuito de proteção limita a tensão de pico de cada célula durante a carga e previne que a tensão da célula caia muito durante a descarga. Além disso, a máxima corrente de carga e descarga é limitada e a temperatura da célula é monitorada para prevenir temperaturas extremas.
O envelhecimento é uma preocupação com a maioria das baterias. Alguma deterioração da capacidade é perceptível após um ano, se a bateria estiver em uso ou não. Acima de dois ou talvez três anos, a bateria frequentemente falha. Outras químicas também têm efeitos degenerativos relacionados à idade, em especial para as baterias de NiMh, se expostas a altas temperaturas ambientes. Armazenar a bateria em um lugar fresco desacelera o processo de envelhecimento da bateria de Li-Ion (e outras químicas).
Além disso, a bateria apenas deve ser parcialmente carregada quando armazenada. Armazenamento prolongado não é recomendado para baterias de Li-Ion. O comprador deve estar ciente da data de fabricação quando comprar baterias de reposição de Li-Ion. Infelizmente, essa informação é frequentemente codificada em um número de série criptografado e está disponível apenas para o fabricante.
A bateria mais econômica à base de lítio, em termos da relação de custo por energia é um conjunto de baterias que usa a célula cilíndrica 18650 (diâmetro = 18 mm e altura = 65 mm). Essa bateria é um tanto volumosa, mas adequada para aplicações portáteis tais como computação móvel.
Se um conjunto de baterias mais fino for necessário (mais fino que 18 mm), a célula prismática de Li-Ion é a melhor escolha.
Quando uma geometria ultrafina é necessária (menor que 4 mm), a melhor escolha é a de lítio-polímero. Essa é a opção mais cara em termos de custo de energia. A bateria de lítio-polímero não oferece ganhos de energia apreciáveis sobre os sistemas de Li-Ion convencionais, nem combina a durabilidade da célula 18650.
As principais vantagens das baterias de Li-Ion são:
- Densidade da energia elevada. Potencial para capacidades ainda maiores.
- Autodescarga relativamente baixa. A autodescarga é menor do que a metade da autodescarga das baterias NiCd e NiMh.
- Manutenção Baixa. Nenhuma descarga periódica é necessária; sem memória.
- Células de Li-Ion causam menos dano quando descartadas do que as de chumbo-ácido ou baterias à base de cádmio. Entre a família de Li-Ion, o manganês é o mais amigável em termos de descarte.
As principais limitações das baterias de Li-Ion são:
- Requer circuito de proteção. O circuito da proteção limita a tensão e a corrente. A bateria é segura se não sobrecarregada.
- Sujeita ao envelhecimento, mesmo se não estiver em uso. Armazenar a bateria em um lugar fresco e a 40% do estado de carga reduz o efeito do envelhecimento.
- Corrente de descarga moderada para alguns tipos.
- Sujeita aos regulamentos do transporte. O embarque de quantidades maiores de baterias de Li-Ion pode estar sujeito ao controle regulador. Esta restrição não se aplica ao carregamento pessoal de baterias.
- Cara de se fabricar. Melhores técnicas de fabricação e recolocação de metais raros com alternativas de custo mais baixo, provavelmente reduzirão o preço.
- Tecnologia não inteiramente madura. As mudanças em combinações do metal e da química afetam resultados de testes nas baterias, especialmente com alguns métodos de testes rápidos.
- Necessitam cuidados, pois as baterias do Li-Ion têm uma alta densidade de energia.
- A alta temperatura resultante do abuso da célula pode causar dano físico.
- O eletrólito é altamente inflamável. A ruptura pode causar a abertura com chama.
